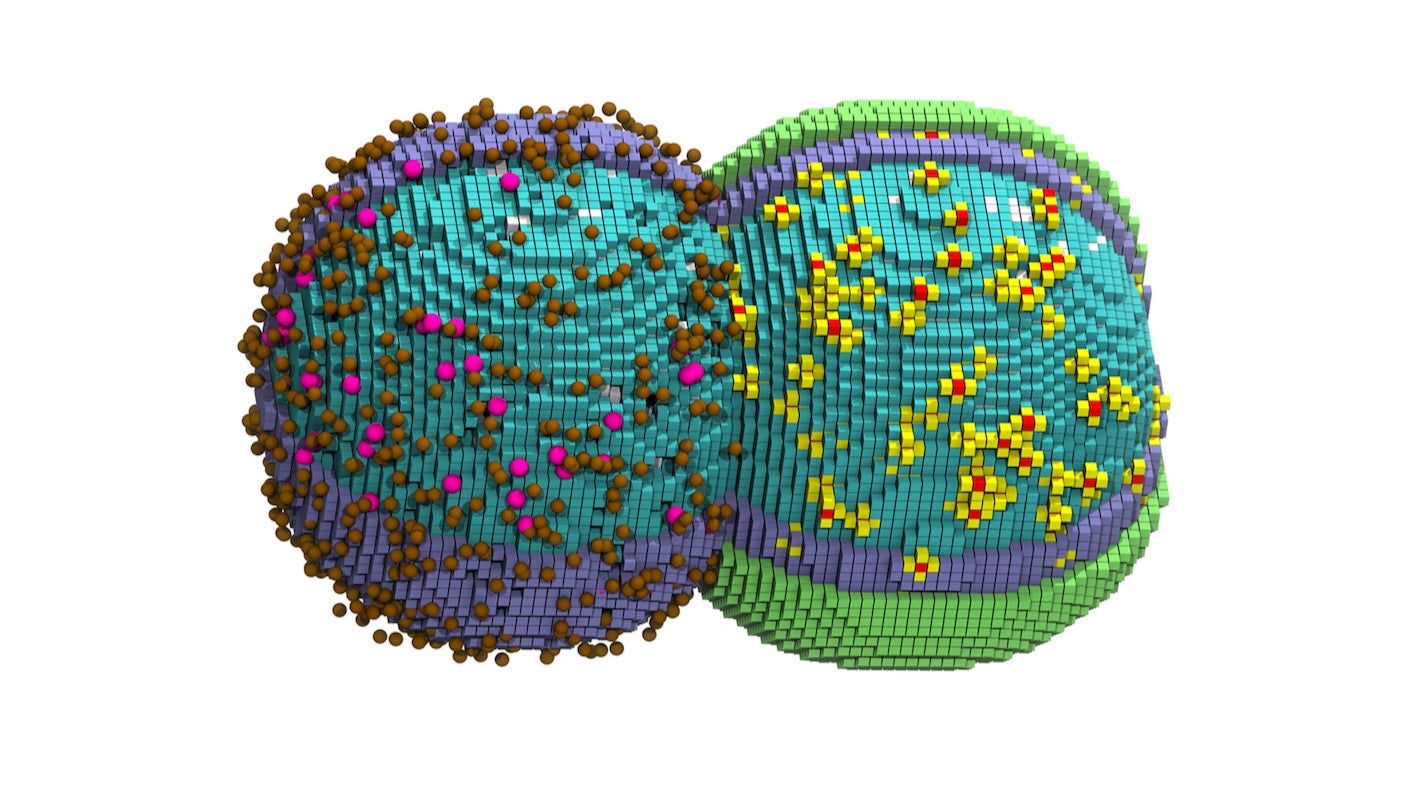

Επιστήμονες στο Πανεπιστήμιο του Ιλινόις δημιούργησαν ένα εικονικό μοντέλο βακτηρίου που προσομοιώνει σχεδόν όλα τα μόριά του σε νανοκλίμακα, καλύπτοντας τον πλήρη κύκλο ζωής του — από την ανάπτυξη ως τη διαίρεση. Η εξέλιξη αυτή ανοίγει νέους δρόμους για την κατανόηση θεμελιωδών βιολογικών διεργασιών και ενδέχεται να επιταχύνει σημαντικά την ανακάλυψη νέων φαρμάκων.
Κάθε κύτταρο είναι μια πολυσύχναστη μητρόπολη. Πρωτεΐνες συντονίζουν εκατοντάδες διεργασίες, μόρια RNA μεταφέρουν οδηγίες από τα γονίδια στα εργοστάσια παραγωγής πρωτεϊνών, και λιπαρά οξέα στη μεμβράνη αναδιατάσσονται συνεχώς για να επιτρέψουν την είσοδο θρεπτικών ουσιών ή να αποκρούσουν εισβολείς. Αυτή ακριβώς η πολυπλοκότητα έκανε την προσομοίωση ενός κυττάρου να μοιάζει για χρόνια με επιστημονική φαντασία.
Τώρα, μια ομάδα ερευνητών στο Πανεπιστήμιο του Ιλινόις στο Urbana-Champaign έκανε ένα βήμα που λίγοι πίστευαν εφικτό: δημιούργησε ένα λεπτομερές ψηφιακό δίδυμο ενός βακτηρίου, το οποίο παρακολουθεί σχεδόν όλα τα μόριά του σε νανοκλίμακα, καλύπτοντας περίπου δύο ώρες πραγματικής βιολογικής δραστηριότητας — δηλαδή έναν πλήρη κύκλο ζωής, από την ανάπτυξη ως τη διαίρεση σε δύο θυγατρικά κύτταρα. Το μοντέλο βασίστηκε στο JCVI-syn3A, ένα συνθετικό βακτήριο με μόλις 493 γονίδια — περίπου τη μισή γονιδιωματική πληροφορία του φυσικού παρασίτου από το οποίο προέκυψε. Είναι ουσιαστικά το πιο απλό γνωστό κύτταρο που μπορεί ακόμα να αναπτυχθεί και να διαιρεθεί κανονικά.
Η πρόκληση δεν ήταν μόνο τεχνική — ήταν θεμελιακά υπολογιστική. Τα υπάρχοντα μοντέλα αντιμετώπιζαν τα κύτταρα ως «καλά ανακατεμένα συστήματα», δηλαδή σαν ένα φλιτζάνι μοριακή σούπα χωρίς χωρική πληροφορία. Αλλά η θέση κάθε μορίου μέσα στο κύτταρο έχει τεράστια σημασία: κάποιες πρωτεΐνες συγκεντρώνονται γύρω από το DNA για να το αντιγράψουν, άλλες κινούνται προς τη μεμβράνη για να διευκολύνουν τη διαίρεση. Αγνοώντας αυτές τις λεπτομέρειες, τα παλαιότερα μοντέλα έχαναν κρίσιμες πληροφορίες.
Η ομάδα χρησιμοποίησε το λογισμικό Lattice Microbes, το οποίο εμπλούτισε με νέα δεδομένα για τις αλλαγές στη μεμβράνη, την κίνηση των ριβοσωμάτων και — το πιο δύσκολο — τη θέση των χρωμοσωμάτων κατά τη διαίρεση, η οποία είναι από τη φύση της τυχαία και δύσκολα προβλέψιμη. Για να αντεπεξέλθουν στις υπολογιστικές απαιτήσεις, χρησιμοποίησαν ξεχωριστές GPU για διαφορετικά τμήματα της προσομοίωσης και απλοποίησαν ορισμένες πρωτεΐνες σε αδρανείς σφαίρες που μπορούσαν να αγνοηθούν σε μεγάλο βαθμό. Αφήνοντας το σύστημα να τρέχει επί μέρες σε supercomputer — συμπεριλαμβανομένης της περιόδου της Ημέρας των Ευχαριστιών — η ομάδα επέστρεψε για να βρει ότι η προσομοίωση είχε ολοκληρωθεί με επιτυχία. «Ξαφνικά, ήταν ένα τεράστιο άλμα», δήλωσε ο Zane Thornburg, ένας από τους συγγραφείς της μελέτης.
Τα αποτελέσματα ταίριαξαν με πραγματικά πειράματα: το μοντέλο αναπαρήγαγε σωστά τον τρόπο που το βακτήριο επιμηκύνεται και παίρνει σχήμα αλτήρα πριν τη διαίρεση, καθώς και τη διάρκεια του κύκλου ζωής του. Επαναλαμβανόμενες προσομοιώσεις με ελαφρώς διαφορετικές αρχικές συνθήκες έδωσαν παρόμοια αποτελέσματα, επιβεβαιώνοντας την αξιοπιστία του μοντέλου.
Το επόμενο βήμα είναι να κατανοήσουμε γιατί ορισμένα γονίδια είναι απολύτως απαραίτητα για τη διαίρεση — κάτι που ακόμα δεν γνωρίζουμε πλήρως. Παράλληλα, η ανάπτυξη εικονικών κυττάρων με generative AI βρίσκεται σε εξέλιξη, αλλά αυτά τα μοντέλα εκπαιδεύονται κυρίως σε δεδομένα γονιδιακής έκφρασης — μια στιγμιαία εικόνα που συχνά αποτυγχάνει να προβλέψει σύνθετες κυτταρικές αντιδράσεις. Η φυσικά θεμελιωμένη προσέγγιση της ομάδας του Ιλινόις και τα AI μοντέλα θα μπορούσαν να αλληλοτροφοδοτηθούν, οδηγώντας σε εικονικά κύτταρα που συμπεριφέρονται όλο και πιο κοντά στα πραγματικά. Το ερώτημα που μένει ανοιχτό: πόσο καιρό θα χρειαστεί για να φτ